
Galvanische Elemente
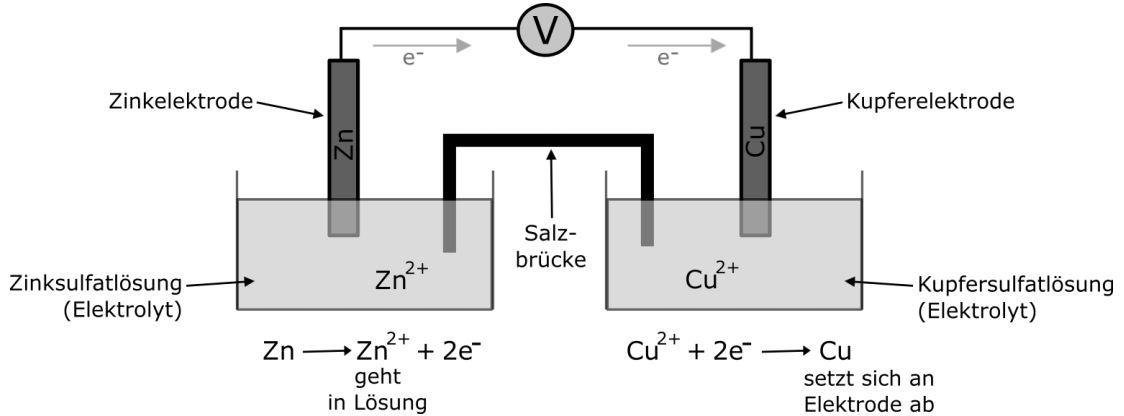
Galvanische Elemente bestehen aus einer Halbzelle eines unedleren Metalls und einer Halbzelle eines edleren Metalls. Das unedlere Metall gibt seine Elektronen gerne ab, wodurch die Zinkatome zu Zink(II)-Ionen reagieren und in Lösung gehen. Die Ionen des edleren Metalls sind bestrebt, Elektronen aufzunehmen um zu dem elementaren Metall zu reagieren. Daher nehmen die Kupfer-(II)-Ionen Elektronen auf und reagieren zu elementarem Kupfer. Die Elektronen, die das Zink abgibt, wandern von der Zinkhalbzelle über den Draht, mit dem die Halbzellen verbunden sind, zu der Kupferhalbzelle, wo sie nun von den Kupfer-(II)-Ionen aufgenommen werden. Es fließt elektrischer Strom.
Die Salzbrücke benötigen wir bei diesem Aufbau, damit ein Ionenaustausch stattfinden kann. Damit werden die Ladungen der beiden Halbzellen ausgeglichen. Das ist notwendig, da sonst die linke Halbzelle immer positiver wird und die rechte immer negativer. Da es auf der Kupferhalbzelle bereits so negativ ist, wandern die Elektronen von der Zinkhalbzelle nicht mehr dorthin.